Pernakah kalian mengamati gula pasir atau garam dapur yang dihaluskan? Butiran –
butiran gula pasir atau garam dapur yang terbentuk apakah masih memiliki sifat gula
atau garam dapur ? Tentunya butiran – butiran tersebut masih memiliki sifat zat
asalnya. Coba kalian perhatikan proses pelarutan gula pasir pada gambar dibawah ini !
Setiap materi,misalnya gula pasir jika ditumbuk sampai halus maka sifat butir-butir
yang terkecil sekalipun masih serupa dengan sifat gula pasir semula, hanya ukurannya
saja yang berubah. Apabila proses pemecahannya diteruskan hasilnya tetap masih
mempunyai sifat-sifat gula pasir. Bahkan ketika dimasukkan dalam airpun rasa manis
gula pasir masih bisa dirasakan.
Butir – butir gula pasir yang terkecil ini pada awalnya dinamakan dengan partikel.
Dengan demikian,setiap materi gula pasir yang kita kenal terdiri atas kumpulan
partikel gula pasir yang jumlahnya banyak sekali. Setiap materi bukan merupakan satu
kesatuan,tetapi merupakan kumpulan dari partikel – partikel yang sangat banyak.
Oleh karena partikel – partikel itu terdiri atas satu kesatuan maka berarti setiap
materi terdiri atas bagian – bagian yang diskontinu (terputus – putus). Pemikiran ini
mendasari pengertian tentang atom yang telah mengalami perkembangan cukup lama.
Teori Atom merupakan salah satu teori yang digunakan untuk mengenali sifat dari
sebuah benda. Menurut sejarah yang tercatat, penemu Teori Atom adalah seorang yang
berasal dari Yunani, yakni Democritus, berikut perkembangan teori atom dari zaman
ke zaman:
- Model Atom Dalton
John Dalton (1776-1844) adalah ilmuwan yang pertama mengembangkan model
atom pada 1803 hingga 1808. Hipotesis Dalton digambarkan dengan model atom sebagai bola pejal seperti tolak peluru. Teori atom Dalton didasarkan pada - anggapan:
- Semua benda tersusun atas atom
- Atom-atom tidak dapat dibagi maupun dipecah menjadi bagian lain
- Atom-atom tidak dapat dicipta maupun dihancurkan
- Atom-atom dari unsur tertentu adalah indentik satu terhadap lainnya dalam
ukuran, massa, dan sifat-sifat yang lain, namun mereka berbeda dari atom-atom
dari unsur-unsur yang lain. - Perubahan kimia merupakan penyatuan atau pemisahan dari atom-atom yang
tak dapat dibagi, sehingga atom tidak dapat diciptakan atau dimusnahkan.

Model Atom Dalton
Namun sayangnya, teori Dalton tidak dapat menjelaskan bagaimana atom sebagai
bola pejal dapat menghantarkan arus listrik. Padahal, listrik adalah elektron yang
bergerak. Ia tak sempat membuktikan partikel lain yang menghantarkan arus listrik.
Secara garis besarnya Teori Dalton memiliki kelemahan antara lain:
- Masih ada partikel sub atomik yang menyusun atom (proton, neutron, elektron)
- Atom atom dari unsur yang sama dapat mempunyai massa yang berbeda
- Tidak mengenal muatan/ sifat listrik materi sehingga tidak bisa menjelaskan
bagaimana cara atom dapat berikatan - Beberapa unsur tidak terdiri dari atom-atom melainkan molekul, seperti molekul
unsur terbentuk dari atom sejenis dengan jumlah tertentu.
- Model Atom Thomson
Pada awal abad ke-20, JJ Thomson menggambarkan atom seperti bola pejal, yaitu
bola padat yang bermuatan positif. Di permukaannya, tersebar elektron yang
bermuatan negatif. Thomson membuktikan adanya partikel yang bermuatan negatif
dalam atom..
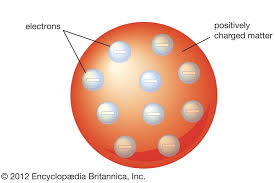
Model Atom Thomson
Namun sayangnya teori atom Thomson juga memiliki kekurangan, yaitu
- tidak adanya lintasan elektron dan tingkat energi.
- tidak dapat menjelaskan susunan muatan positif dan negatif dalam atom.
- Model Atom Rutherford
Ernest Rutherford, ahli fisika kelahiran Selandia Baru adalah salah satu tokoh yang
berjasa dalam pengembangan model atom. Rutherford membuat model atom
seperti tata surya.
- Atom adalah bola berongga yang tersusun dari inti atom dan elektron yang
mengelilinginya. - Inti atom bermuatan positif. Selain itu, massa atom terpusat apda inti atom.
Model ini persis seperti bagaimana planet mengelilingi matahari. Rutherford berjasa
mengenalkan konsep lintasan atau kedudukan elektron yang kelak disebut dengan
kulit atom. Namun model atom Rutherford tidak dapat menjelaskan mengapa
elektron tidak jatuh ke dalam inti atom
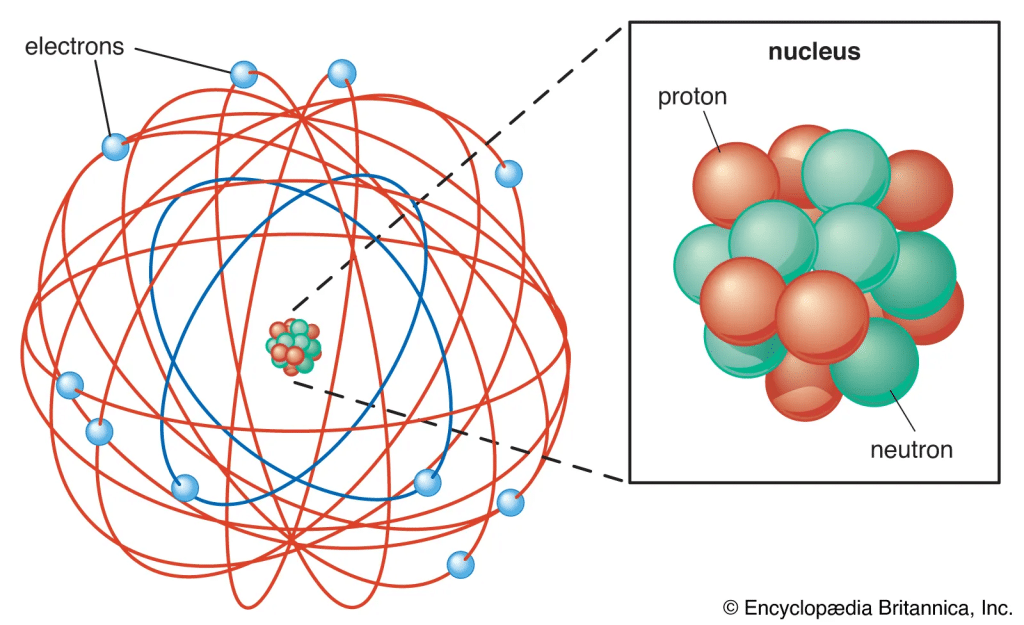
Model Atom Rutherford
- Model Atom Niels Bohr
Niels Bohr, ahli fisika dari Denmark adalah ilmuwan pertama yang mengembangkan
teori struktur atom pada 1913. Teori tentang sifat atom yang didapat dari
pengamatan Bohr:
- Atom terdiri dari inti yang bermuatan positif dan dikelilingi oleh elektron yang
bermuatan negatif di dalam suatu lintasan. - Elektron bisa berpindah dari satu lintasan ke lintasan yang lain dengan
menyerap atau memancarkan energi sehingge energi elektron atom itu tidak
akan berkurang - Jika berpindah ke lintasan yang lebih tinggi, elektron akan menyerap energi.
- Jika berpindah ke lintasan yang lebih rendah, elektron akan memancarkan
energi.
Kedudukan elektron-elektron pada tingkat-tingkat energi tertentu yang disebut
kulit-kulit elektron.
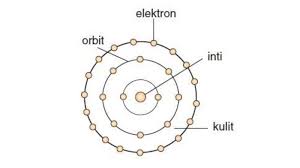
Model atom Niels Bohr
menunjukkan bahwa atom terdiri dari beberapa kulit. Kulit ini adalah tempat
berpindahnya elektron. Kesimpulan yang diperoleh adalah selama elektronelektron berada di lintasan energinya relatif tetap. Elektron-elektron yang berputar
mengelilingi inti atom berada pada lintasan atau tingkat energi tertentu yang
kemudian dikenal dengan sebutan kulit atom. Dasar inilah yang digunakan untuk
menentukan konfigurasi elektron suatu atom.Namun model atom Bohr memiliki
Kelemahan,yaitu :
- Adanya radius dan orbit. Ini tidak sesuai dengan Prinsip Ketidakpastian
Heisenberg yang menyatakan radius tidak bisa ada bersamaan dengan orbit. - Selain itu, model atom Bohr juga tidak menjelaskan Efek Zeeman. Efek Zeeman
adalah ketika garis spektrum terbagi karena adanya medan magnet
- Model Atom Mekanika Kuatum
Setelah abad ke-20, pemahaman mengenai atom makin terang benderang. Model
atom modern yang kita yakini sekarang, telah disempurnakan oleh Erwin
Schrodinger pada 1926. Schrodinger menjelaskan partikel tak hanya gelombang,
melainkan gelombang probabilitas. Kulit-kulit elektrin bukan kedudukan yang pastu
dari suatu elektron, namun hanya suatu probabilitas atau kebolehjadian saja.
Sebelumnya, Werner Heisenberg juga mengembangkan teori mekanika kuantum
dengan prinsip ketidakpastian. Prinsip tersebut kurang lebih berbunyi: “Tidak
mungkin dapat ditentukan kedudukan dan momentum suatu benda secara seksama
pada saat bersamaan, yang dapat ditentukan adalah kebolehjadian menemukan
elektron pada jarak tertentu dari inti atom.” Awan elektron di sekitar inti
menunjukkan tempat kebolehjadian ditemukannya elektron yang disebut orbital
dimana orbital menggambarkan tingkat energi elektron. Orbital-orbital dengan
tingkat energi yang sama atau nyaris sama akan membentuk sub-kulit. Kumpulan
beberapa sub-kulit akan membentuk kulit. Dengan demikian, kulit terdiri dari
beberapa sub-kulit, dan sub-kulit terdiri dari beberapa orbital.
Model atom dengan orbital lintasan elektron ini disebut sebagai model atom
modern atau model atom mekanika kuantum yang berlaku hingga saat ini
Secara singkat Perkembangan model atom dapat dituliskan sebagai berikut:
- Dalton menyarankan bahwa atom adalah bagian terkecil dari materi yang tidak bisa
dibagi-bagi lagi. - Thomson menyatakan bahwa atom adalah partikel positif dengan elektron yang
tersebar di dalamnya.
- Rutherford menyatakan bahwa atom terdiri dari inti atom yang bermuatan positif
dan dikelilingi elektron yang bermuatan negatif. - Neils Bohr menyarankan bahwa elektron yang berputar mengelilingi atom berada
pada lintasan atau tingkat energi tertentu. - Mekanika Kuantum menemukan daerah kebolehjadian ditemukannya elektron yang
dinamakan dengan orbital
Setelah kegiatan pembelajaran 1 ini diharapkan kalian akan mampu membandingkan
perkembangan teori atom mulai dari teori atom Dalton hingga teori atom Mekanika
Gelombang
